تمامی اجزا کیت استخراج در 16-25 °C قابل نگهداری هستند به جز برخی مواد مصرفی داخل کیت ها که در جدول پایین به آن ها اشاره شده است.
در صورت رعایت این شرایط تمامی مواد تا زمان انقضا پایدار می باشند.
نام ماده | شرایط انتقال | شرایط نگهداری |
P.K (Lyophilized) | 16-25 °C (< 30 mins) | -20 °C |
P.K Buffer | RT | 2-8 °C |
Lysozyme (Lyophilized) | 16-25 °C (< 30 mins) | 2-8 °C |
Lysozyme Buffer | RT | 2-8 °C |
Carrier | RT | 2-8 °C |
به منظور استخرا از نمونه های Urine, Amniotic Fluid, Thin prep,... در صورتی که از تعداد سلول کافی برخوردار نبودند، پیشنهاد میگردد کل حجم نمونه را در فالکون ریخته و رسوب سلولی تهیه شود.
همچنین می تواند مرحله سانتریفیوژ پس از انکوباسیون 20 دقیقه ای در 56 °C را نیز حذف نمایید.
در جدول زیر، دو کیت فوق مقایسه شده اند.
متغیرها | کیت استخراج Viral RNA | کیت استخراج Modified Viral RNA |
نوع نمونه | سرم، پلاسما، CSF، مایعات بدن، نمونه حلق و بینی | نمونه های حلق وبینی |
زمان استخراج به ازای هر تست | 20 | 10 |
ویروس های قابل بررسی | HIV, Covid-19, HCV, Flu, RSV & other types of RNA viruses | Covid-19, Flu, RSV & other Upper Respiratory Tract viruses |
ویژگی | قابلیت استخراج محدوده وسیعی از ویروس های دارای ژنوم RNA از انواع نمونه ها | دارای محلول نمونه گیری که همزمان با نمونه گیری، عمل لیز و غیرفعال کردن ویروس را نیز انجام می دهد. قابلیت نگهداری نمونه در محلول مخصوص آن تا 48 ساعت در شرائط دمای اتاق (16-25 درجه) |
بافرهای AW1 و AW2 به صورت آماده در داخل کیت قرار داشته و نیازی به آماده سازی این بافرها توسط کاربر در آزمایشگاه نمی باشد. لذا در صورتی که شرایط نگهداری مطابق با برچسب مندرج بر روی ظرف حاوی بافر رعایت شود، تا زمان پایان انقضا، پایدار است.
متغیرها | Viral RNA | Viral Nucleic Acid |
نوع نمونه | سرم، پلاسما، CSF، مایعات بدن، نمونه حلق و بینی و ... . | سرم، پلاسما، CSF، مایعات بدن، نمونه حلق و بینی و ... . |
زمان استخراج به ازای 1 نمونه | 20 | 30 |
ویروس های قابل بررسی | HIV, Covid-19, HCV, Flu, RSV & other types of RNA viruses | HBV, HCV, HIV, Covid-19, Flu & other types of Viral RNA/ DNA |
ویژگی | قابلیت استخراج محدوده وسیعی از ویروس های دارای ژنوم RNA از انواع نمونه ها | قابلیت استخراج DNA/ RNA ویروسی از انواع نمونه ها
|
*** ترجیحا به منظور استخراج RNA ویروس ها مثل HCV, HIV به منظور شناسایی دقیق تر ویروس در تیترهای پایین از کیت Viral Nucleic Acid Extraction استفاده نمایید.
خیر. هپارین در نمونه های حاوی هپارین (نمونه گیری در لوله هپارین، بیمار مصرف کننده هپارین) به عنوان یک عامل مهارکننده PCR شناخته شده و عمل می کند.
خیر، از این محلول صرفا در صورتی که نمونه مورد استفاده خلط (Sputum) است، استفاده شود.
اشکال فوق در اکثر مواقع عملا رخ میدهد. برای به دست آوردن حد اکثر سلول، پیشنهاد می شود به منظور از دست ندادن رسوب به هنگام خارج نمودن سوپرناتانت به شرح زیر انجام دهید:
نمونه را در یک میکروتیوب 1.5 ml منتقل نموده و مطابق با دستورالعمل کیت سانتریفیوژ نمایید، پس از خارج نمودن سوپرناتانت، مابقی نمونه را بر روی رسوب ریخته و مطابق با دستورالعمل سانتریفیوژ کنید. این عمل را تا زمانی که کل حجم نمونه تمام شود تکرار کنید.
همچنین، برای استخراج از مایع آمنیوتیک و ادرار، انجام سانتریفیوژ در 10,000 xg به مدت 3 دقیقه که پس از انکوباسیون در 60 °C انجام می شود، لازم نیست.
بله، در صورتی که نمونه در 2-8 °C و یا -20 °C نگهداری شده باشد، این عمل بلامانع است.
بله، در صورتی که نمونه بافت غیر پارافینه در محلولی غیر از فرمالین نگهداری می شود، مرحله انکوباسیون در 95 °C حذف می شود.
در صورتی که نمونه دارای سلول مثل ترشحات زخم و یا سلول های دهان در حال بررسی است، پیشنهاد می شود که از نمونه، رسوب تهیه شده و بر اساس تصویر زیر آماده سازی نمونه انجام شود.
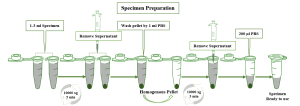
در صورتی که در نمونه thin prep، سلول ناکافی بود، در وهله اول تکرار نمونه گیری پیشنهاد می شود، در غیراینصورت، کل حجم نمونه را در لوله فالکون ریخته و مطابق نحوه تهیه رسوب از ادرار عمل نمایید.
خیر، در صورت بروز این مورد، نیازی به تکرار استخراج نمی باشد.
بله، ولی لازم به ذکر است که در صورت مخلط کردن دو محلول فوق، محاسبه حجم حتما صورت بگیرد تا نسبت ها بهم نریخته و متعادل گردد. همچنین، پس از مخلوط کردن این دو محلول، Lysis Buffer در دمای RT نگهداری شود.
بله. در صورت مشاهده رسوب در بافرها، آن ها را در حمام آب 56 °C قراردهید تا رسوب حل شود.
در صورت مشاهده رسوب، نمونه را در 6800 xg به مدت 3 دقیقه سانتریفیوژ نموده و سوپرنانات را به یک تیوب منتقل و عمل استخراج را انجام دهید.
در صورتی که حجم نمونه مناسب نبود، با افزودن مقدار مناسب از PBS، حجم نمونه را به 200 µl برسانید.
زنان: نمونه های thin prep، ادرار صبح گاهی (ادرار در زنان در صورتی پیشنهاد می وشد که فرد، باکره و یا دچار واژینیسموس باشد).
مردان: نمونه ادرار صبحگاهی به همراه نمونه گیری از اندام تناسلی
خیر. استخراج از نمونه wart با کیت Paraffin-wax DNA Extraction باید انجام شود، به دلیل اینکه این کیت حاوی یک بافر مخصوص برای استخراج بافت است. باید توجه داشت در صورتی که نمونه wart در محیطی غیر از فرمالین قرار دارد، مرحله انکوباسیون در 95 °C حذف شود.
خیر، در صورت مشاهده رسوب و یا بافت لیز نشده پس از مرحله لیز، اتانول را به مخلوط نمونه و لیز افزوده و پس از ورتکس کردن در صورت برطرف نشدن رسوب، آن را در 10,000 xg به مدت 3 دقیقه سانتریفیوژ نموده و از سوپرناتانت برای مراحل بعدی استفاده نمایید.
از آن جا که نمونه ادرار این بیماران دارای رسوب زیادی هستند پیشنهاد می شود در مرحله اول تهیه رسوب، به جای استفاده از فالکون برای تهیه رسوب، نمونه را در میکروتیوب 1.5 ml سانتریفیوژ نمایید.
چنانچه تهیه رسوب در 2 میکروتیوب انجام شده است و مقدار رسوب قابل توجه باشد، پیشنهاد می شود صرفا از رسوب تشکیل شده در یک میکروتیوب برای ادامه استخراج استفاده شود. اگر پس از افزودن 200 µl از PBS به رسوب، نمونه غلیظی حاصل شد، نمونه را در مقدار بیشتری از PBS رقیق کرده و سپس ادامه استخراج را انجام دهیدپ
خیر، زیرا نتیجه به دست آمده نامعتبر است و ممکن است نتایج منفی کاذب را نیز در تیتر پایین ویروس مشاهده نمایید.
خیر. وجود خون در نمونه دال بر عدم دسترسی به نتیجه مناسب نیست. به منظور دسترسی به نتیجه معتبر در صورتی که تمام پروتکل به درستی اجرا شود و با توجه به حساس بودن نمونه مایع آمنیوتیک و عدم امکان نمونه گیری مجدد از مادر، پیشنهاد میگردد در مرحله Lysis مقدار 10 µl از Carrier RNA را به نمونه به همراه Binding Buffer و P.K اضافه نموده و در نهایت به منظور دسترسی به DNA، مرحله Elution را در دو مرحله تکرار نمایید، یعنی به جای آنکه 100 µl از Elution Buffer را در یک مرحله اضافه کنید، این بافر را در دو مرحله و در مرحله 50 µl بر روی ستون ریخته و در هرمرحله سانتریفیوژ نمایید.
بله. در صورت بروز خطا، حتما باید تکرار استخراج صورت بپذیرد تا نتیجه معتبر حاصل شود.
در صورتی که بلافاصله پس از افزودن AW2 به جای AW1 کاربر متوجه خطا شود، می تواند پس از سانتریفیوژ در 8,000 rpm به مدت 1 دقیقه، مراحل شستشو را از ابتدا تکرار نماید ولی درصورت اتمام فرآیند استخراج، تست باید تکرار شود.
خیر، با توجه به حجم زیاد نمونه Thin prep و همچنین بعضا عدم وجود سلول کافی در نمونه، امکان دستیابی به نتایج منفی کاذب زیاد است.
با توجه به تجربه بدست آمده از کنترل کیفی های انجام شده بر روی بیش از 2000 نمونه HPV، فازغ از نوع کیت استخراج، رعایت نکات ارائه شده در راهنمای کیت لازم به اجرا است.
بله استخراج قطعات با اندازه 1 kb با استفاده از Genomic DNA Purification Kit امکان پذیر است.
به منظور استخراج باکتری Nocardia از کیت ABG MTB DNA Extraction با رعایت تمامی مراحل پروتمل استفاده نموده و مرحله انکوباسیون در 95 °C به مدت 1 ساعت را حذف نمایید.


